Introduktion
Jag har varit där du är – stirrat på en bildskärm klockan 02.00, sett en baslinje som driver som en förlorad båt till havs, undrar om "HPLC doo-hickey" uppfanns bara för att testa mitt förstånd. Om du känner dig förvirrad när du försöker linda huvudet runt högpresterande vätskekromatografi (HPLC), ta ett andetag. Det är inte bara en låda med dyra delar; det är en delikat dans mellan kemi och fysik.
I labbet säger vi ofta att den mobila fasen är systemets "livlinje". Utan det sitter ditt prov bara i en injektor och går ingenstans. Men hur väljer du rätt "tåg" för att bära dina molekyler till detektorn? Låt oss bryta ner det som om vi pratar över en kaffe i pausrummet.
1. Vad är HPLC, egentligen?
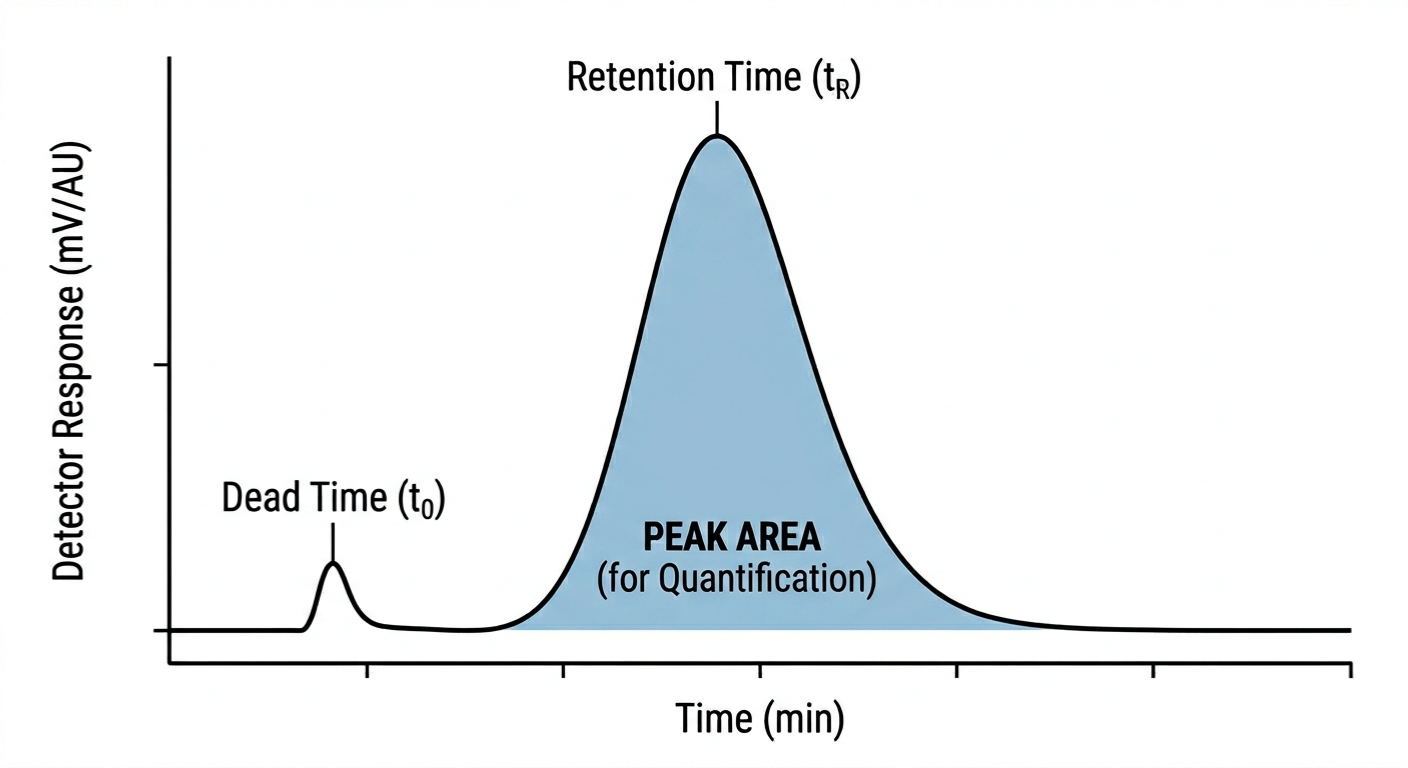
I sin kärna handlar HPLC om separation. Se det som ett lopp där "banan" är den stationära fasen (kolonnen) och "vinden" som driver löparna längs är den mobila fasen av hplc.
Magin uppstår eftersom olika molekyler har olika "affiniteter". Vissa molekyler älskar den mobila fasen och zoomar igenom kolonnen. Andra är "klibbiga" - de är kära i den stationära fasen och ligger efter. Denna skillnad i hastighet är det som skapar dessa toppar på ditt kromatogram.
2. Normal fas vs. omvänd fas
Det är vanligtvis där alla börjar dra ut håret. Under mina år av praktik har jag hittat det enklaste sättet att komma ihåg detta genom att titta på polaritet.
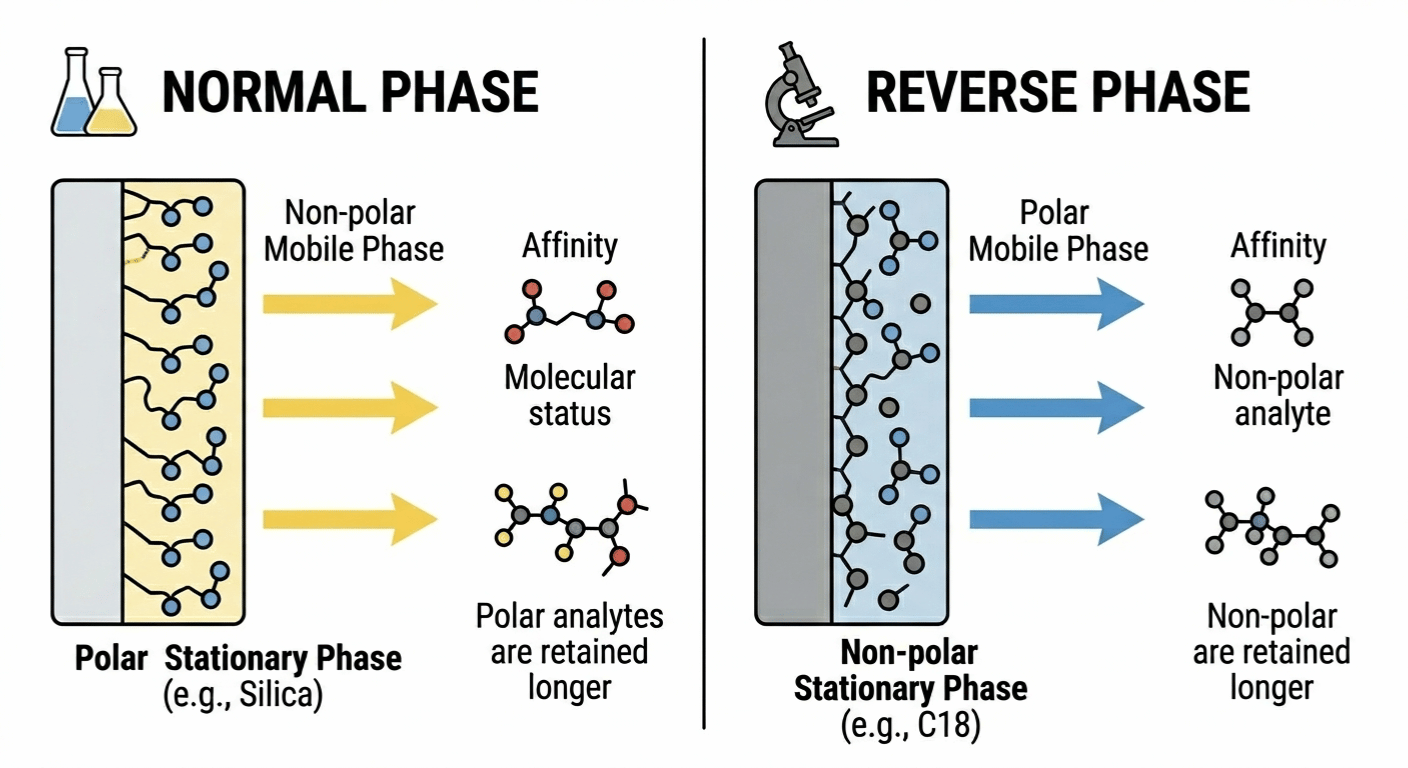
A. Normalfaskromatografi
Detta är "old school" sättet. I normalfaskromatografi är den stationära fasen polär - tänk på den som en magnet för polära molekyler. Den mobila fasen vi använder här är opolär, vanligtvis lösningsmedel som hexan eller heptan.
-
Logiken: Polära "klibbiga" molekyler hålls tillbaka av den polära kolonnen. Icke-polära molekyler tvättas ut snabbt med den opolära mobila fasen.
-
Proffstipset: Om du ökar polariteten på din mobila fas (tillsätter lite isopropanol) kommer dina prover faktiskt att röra sig snabbare.
B. Omvänd faskromatografi
Idag är detta guldstandarden. Förmodligen involverar 90% av det arbete jag gör i labbet omvänd faskromatografi. Här vänder vi manuset. Kolonnen är opolär (hydrofob, som olja), och den rörliga fasen är polär (vanligtvis en blandning av vatten och metanol eller acetonitril).
-
Logiken: Vattenälskande (polära) molekyler zoomar igenom eftersom de hatar den oljiga kolonnen. Fettälskande (icke-polära) molekyler fastnar på kolonnen som lim.
-
Varför vi älskar det: Det är förutsägbart, mångsidigt och använder vattenbaserade lösningsmedel som är lättare att hantera.
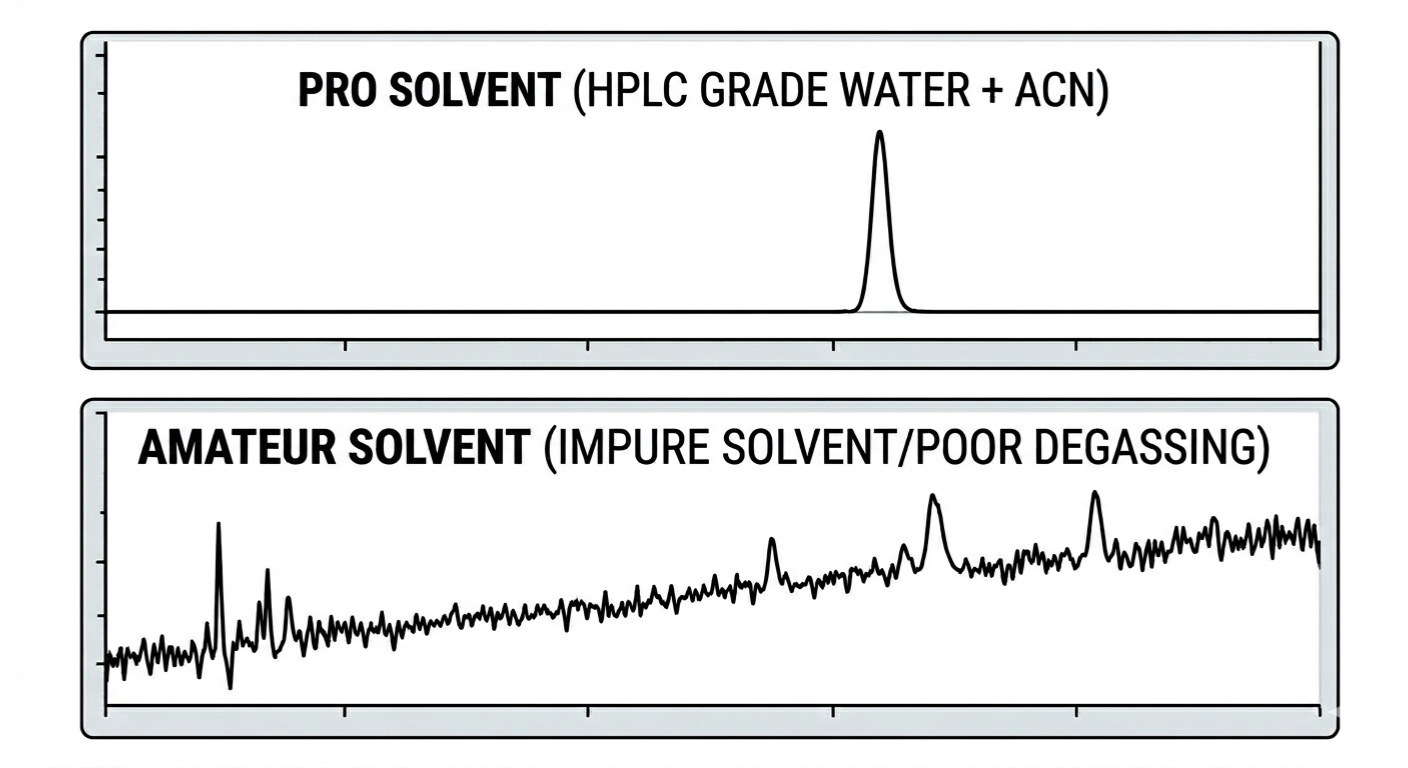
3. Den "gyllene regeln" för lösningsmedelskvalitet
Du kommer att se "HPLC Grade" på etiketterna av en anledning. Tänk inte ens på att använda ACS-klass eller något mindre. Varför? Eftersom dessa "små" föroreningar i lösningsmedel av lägre kvalitet kommer att ackumuleras på din kolumn med tiden, vilket dödar din upplösning och skapar konstiga spöktoppar.
Använd alltid vatten av typen Milli-Q (18,2 MΩ.cm). Om ditt vatten är "smutsigt" kommer din baslinje att se ut som en bergskedja, och du kommer att spendera tre dagar på att försöka ta reda på varför.
4. Avgasning och filtrering: The Performance Killers
Luft är fienden till hplc:s mobila fas. Under normalt tryck löses luft i dina lösningsmedel. Men när lösningsmedlet väl träffar pumpen kan de små bubblorna fastna i backventilerna eller detektorcellen.
-
Resultatet: Flödeshastighetsfluktuationer, pulserande baslinjer och rörliga retentionstider.
-
Fix: Använd inbyggda avgasare eller ultraljud\/vakuumfiltrering om du kör högkänsliga analyser.
Filtrering är inte valfritt. Även lösningsmedel av HPLC-kvalitet kan ha mikroskopiska partiklar från tillverkningsprocessen eller flasklocket. Filtrera alltid genom ett 0,22 µm eller 0,45 µm membran innan det vidrör din reservoar. Det är en 5-minutersuppgift som kan rädda din kolumn från en för tidig död.
5. Buffertar och glasfällan
I omvänd faskromatografi använder vi buffertar för att hålla pH stabilt för joniserbara prover.
-
Proffstips: Om du använde en buffert idag, tvätta systemet med rent vatten\/organisk mix innan du går hem. Om du inte gör det kommer dessa salter att kristallisera och riva dina pumptätningar.
-
Glasfällan: Visste du att om pH i din hplc mobilfas är > 8,0 kan den faktiskt läcka ut metalljoner från glasreservoarer? Byt till behållare av rostfritt stål eller specialplast i dessa fall.
Låt oss få din separation perfekt
Att få den mobila fasen rätt är 80 % av striden i HPLC. Om du kämpar med "shag matta" baslinjer, tryckspikar eller inkonsekventa resultat, slösa inte en dag till med att gissa.
Jag har tillbringat tusentals timmar vid bänken för att felsöka dessa exakta problem. Jag delar alltid gärna med mig av lite "labbevisade" råd för att få ditt projekt på rätt spår igen.
Referenser
-
Snyder, L.R., Kirkland, J.J., & Dolan, J.W. (2011). Introduktion till modern vätskekromatografi. 3:e upplagan. John Wiley & Sons. ("Guldstandarden" för att förstå HPLC-separationsmekanismer).
-
Dolan, J.W. (2002). "Mobil fasförberedelse." LCGC Nordamerika, Felsökningsserien. (Viktig praktisk guide för avgasning och filtrering).
-
Aparicio, R. (Red.). (2013). Manual för HPLC-optimering. Elsevier. (Omfattande data om lösningsmedelspolaritet och buffertval i omvänd faskromatografi).
-
Agilent Technologies. "HPLC-systemfelsökningsguide: Undvika vanliga mobilfasfel." Tekniskt resursbibliotek.
-
Waters Corporation. "Principer för kromatografi: normal fas vs. omvänd fas." Utbildningsserien.
-
Internationell konferens om harmonisering (ICH). Q2(R1) Validering av analytiska procedurer: text och metodik. (Standard för peak area kvantifiering och retentionstid stabilitet).


 engelska
engelska kinesiska
kinesiska