W nowoczesnym laboratorium analitycznym chromatografia to znacznie więcej niż rutynowy protokół; jest to skomplikowany taniec interakcji molekularnych. Niezależnie od tego, czy oznaczasz ilościowo zanieczyszczenia farmaceutyczne, czy wykrywasz zanieczyszczenia środowiska w ilościach śladowych, zrozumienie podstawowych zasad fizyki separacji jest tym, co odróżnia technika od mistrza chromatografa.
Sukces w laboratorium nie zależy tylko od ustawień najwyższej klasy instrumentów. Opiera się na synergii pomiędzy chemią metody i wysokiej jakości materiałami eksploatacyjnymi, które chronią integralność próbki. Dla tych, którzy poruszają się po zawiłościach
HPLC vs LC-MS: co wybrać
lub zmagających się z niestabilnymi wartościami bazowymi, w tym przewodniku opisano praktyczne sekrety uzyskiwania danych światowej klasy i maksymalizowania czasu pracy przyrządu.
Zrozumienie hydrofobowego uścisku dłoni: co to jest chromatografia z odwróconą fazą?
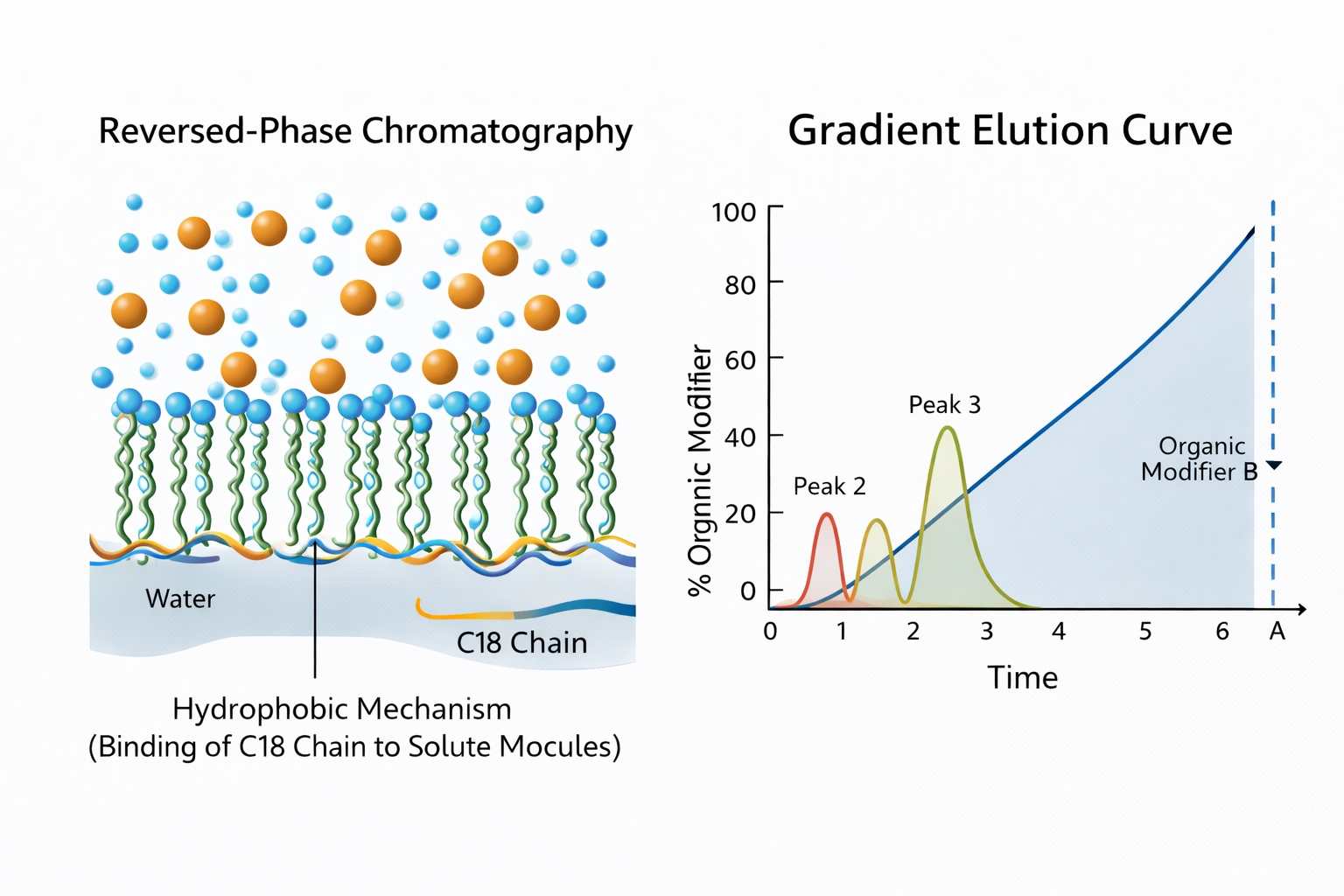
Aby odpowiedzieć na podstawowe pytanie – czym jest chromatografia z odwróconą fazą – należy wyjść poza podręcznikową definicję. W swej istocie jest to separacja oparta na „strachu przed wodą” (hydrofobowość). W wysokociśnieniowej chromatografii cieczowej z odwróconymi fazami (RP-HPLC) wykorzystujemy niepolarną fazę stacjonarną i polarną fazę ruchomą do sortowania cząsteczek według ich hydrofobowego charakteru.
Chemia łańcucha C18 (oktadecylu).
Najbardziej powszechną fazą stacjonarną są cząstki na bazie krzemionki połączone łańcuchami C18 (oktadecylowymi). Z mojego doświadczenia wynika, że gęstość łańcuchów C18 i jakość nośnika krzemionkowego decydują o wytrzymałości Twojej metody. Wielu analityków napotyka ogonowanie pików podczas analizy związków podstawowych. Jest to często spowodowane resztkowymi grupami silanolowymi na powierzchni krzemionki, które działają jako niepożądane miejsca wymiany jonowej.
Aby rozwiązać ten problem, używamy kolumny z końcówką, w której mniejsze silany „maskują” te miejsca aktywne. Jednak nawet najlepsza kolumna nie naprawi słabego wtrysku. Jeśli pik chromatograficzny wygląda na zniekształcony, zanim w ogóle dotrze do kolumny, sprawdź fiolkę. Używanie wysokiej czystości
Fiolki z krótkim gwintem 9 mm i uniwersalnym dopasowaniem
gwarantuje, że analit nie adsorbuje się na ściankach fiolki, zanim igła go złapie.
Sztuka modyfikatora organicznego w opracowywaniu metody HPLC
Czas retencji analitów zależy od stężenia organicznego modyfikatora HPLC. Dostosowując stosunek acetonitrylu lub metanolu do buforu wodnego, regulujesz „siła elucji” fazy ruchomej.
Częstą pułapką, jaką widzę w transferze metod, jest źle rozumiana krzywa elucji gradientowej. Jeśli zbyt szybko zwiększysz modyfikator organiczny, stracisz rozdzielczość; zbyt wolno i cierpisz z powodu poszerzania pików i marnowania rozpuszczalnika. Podczas przełączania pomiędzy
Analityczna i preparatywna HPLC
zarządzanie nachyleniem gradientu staje się głównym czynnikiem pomyślnego zwiększania skali. Pamiętaj, że acetonitryl oferuje niską lepkość i wysoką siłę elucji, podczas gdy metanol może zapewnić różną selektywność w przypadku związków polarnych, których ACN może nie zauważyć.
Rozszyfrowanie kolejności elucji GC: przewidywanie rozdziału związków
Przewidywanie kolejności elucji gc jest jednym z najbardziej satysfakcjonujących wyzwań dla chromatografa gazowego. W przeciwieństwie do HPLC, gdzie główną dźwignią jest chemia rozpuszczalnika, separacja GC jest podyktowana „trójcą separacji”: temperaturą wrzenia, polarnością molekularną i programowaniem temperatury kolumny.
Termodynamika a oddziaływania dipolowe
W niepolarnej fazie stacjonarnej kolejność elucji gc jest ściśle zgodna z temperaturą wrzenia. Najpierw wychodzą bardziej lotne związki. Jednak sytuacja się zmienia, gdy używasz kolumny polarnej, takiej jak PEG\/Wax. Niedawno zajmowałem się projektem obejmującym izomery, których temperatury wrzenia były prawie identyczne. Przechodząc do fazy polarnej, interakcje dipol-dipol pozwoliły nam rozdzielić te związki na podstawie ich struktury elektronowej, a nie rozmiaru.
W przypadku prac o wysokiej czułości, takich jak analiza śladów środowiskowych, integralność pojemnika na próbkę ma ogromne znaczenie. Używanie
Fiolki z zagniataną końcówką o średnicy 20 mm
zapobiega utracie lotnych analitów, zapewniając, że dekonwolucja widma masowego opiera się na prawdziwej reprezentacji próbki, a nie na frakcji, która wyciekła.
HPLC vs LC-MS: poruszanie się po zmianie czułości
Częstym pytaniem w naszym laboratorium jest: „Kiedy powinniśmy przejść z HPLC na LC-MS?” Odpowiedź leży w wymaganej wrażliwości. Podczas gdy HPLC z detekcją UV doskonale nadaje się do rutynowej kontroli jakości na poziomie mikrogramów, LC-MS jest wymagana, gdy trzeba wykryć poziomy pikogramów lub zidentyfikować niewiadome w złożonych matrycach.
Jeśli przechodzisz na LC-MS, wybór fiolek staje się jeszcze ważniejszy. Standardowe czapeczki mogą przedostać się plastyfikatory do fazy ruchomej, tworząc „duch szczytów”, które nawiedzają chromatogram. Dlatego właśnie Aijiren’s
Klejone zakrętki
stanowią podstawę laboratoriów posiadających certyfikat MS — eliminują ryzyko wpadnięcia przegród do fiolki lub przedostania się zanieczyszczeń do detektora.
Anatomia doskonałego piku chromatograficznego
Każdy pik chromatograficzny jest narzędziem diagnostycznym. Ostry, symetryczny pik Gaussa informuje, że system jest zoptymalizowany. „Ramię” lub „ogon” informuje, że coś jest nie tak, często związane ze sprzętem lub martwą głośnością.
Eliminowanie objętości martwej i objętości pozakolumnowej
Jednym z cichych zabójców rozdzielczości jest martwa głośność. Jeśli pomiędzy igłą a dnem fiolki istnieje szczelina, próbka ulega rozproszeniu. Do mikropróbkowania zawsze polecam stosowanie wkładek stożkowych. Wkładki te wpychają próbkę w wąską, pionową ścieżkę, zapewniając wtrysk „ostrego czopa”. To bezpośrednio skutkuje ostrzejszym szczytem i lepszym stosunkiem sygnału do szumu, szczególnie w systemach wysokociśnieniowych, gdzie wrogiem jest dyspersja.

Rozwiązywanie problemów jak profesjonalista: od szumu podstawowego do rdzenia przegrody
W ciągu wielu lat rozwiązywania problemów odkryłem, że 70% problemów z instrumentami to w rzeczywistości problemy z materiałami eksploatacyjnymi.
-
Szum bazowy i szczyty duchów: Jeśli widzisz szczyty tam, gdzie nie powinno ich być, przyczyną mogą być Twoje filtry. Zawsze odsyłaj
Kompletny przewodnik po filtrach 0,22 mikrona
przed wyborem filtrów strzykawkowych.
-
Septa Coring: Jeśli widzisz kawałki silikonu w fiolce, oznacza to, że igła „wbija” przegrodę. Dzieje się tak w przypadku czapek złej jakości. Nasze nasadki zaciskane ND11 i nakrętki 10-425 są precyzyjnie zaprojektowane, aby wytrzymać wielokrotne przebicia bez fragmentacji.
-
Stabilność podczas przechowywania: Do metod EPA lub długotrwałego przechowywania przy użyciu
24-400 fiolek EPA
wykonany ze szkła borokrzemianowego zapewnia zerową utratę rozpuszczalnika i zero zanieczyszczeń.
Dlaczego integralność danych zaczyna się od materiałów eksploatacyjnych
Często wydajemy 50 000 dolarów na wysokiej klasy system, a potem staramy się zaoszczędzić grosze na fiolce. Z mojego doświadczenia wynika, że kiepska fiolka jest najdroższą rzeczą w twoim laboratorium, ponieważ prowadzi do „ponownych badań” i „nieudanych walidacji”.
Niezależnie od tego, czy potrzebujesz 1 ml fiolek z osłoną do prostej chromatografii, czy 18 mm fiolek z gwintem typu Headspace do automatycznej GC, Aijiren zapewnia konsystencję, której wymagają eksperci. Dbamy o to, aby kolejność elucji gc była powtarzalna dzień po dniu, a pik chromatograficzny pozostał tak ostry, jak w dniu opracowania metody.
Wsparcie ekspertów i zapytania: Czy napotykasz niespójne wyniki lub masz problemy z rozwojem metody? Razem zoptymalizujmy Twój przepływ pracy. Skontaktuj się ze mną w celu konsultacji technicznej:
Podsumowanie Opanowanie zjawiska odwróconej fazy i niuansów instrumentu to podróż polegająca na ciągłym uczeniu się. Wybierając odpowiedni organiczny modyfikator HPLC i najlepsze w swojej klasie materiały eksploatacyjne, inwestujesz w prawdziwość swoich danych. Nie pozwól, aby kiepska fiolka zrujnowała genialną metodę, nad którą pracowałeś tygodniami.


 Angielski
Angielski chiński
chiński

